洁净室的分类方法很多,按照洁净室的使用性质我们一般划分为三类:工业洁净室、一般生物洁净室和生物安全实验室(洁净室) 。一般生物洁净室主要控制有生命的微粒子对操作对象的污染,装饰材料要能够经受各种灭菌剂的侵蚀,通过暖通工程系统的配置将空间内部保持正压。这就区别了生物安全实验室(生物安全洁净室),后者是除了要求控制有生命的微粒对操作对象的污染外,还要求控制具有潜在危害的操作对象对操作人员及周围环境的污染,对压差的控制更为重要,室内需保持负压。>>>商务洽谈,点此处,在线咨询
生物药车间的建设如果对洁净室认知不全面,很难通过竣工验收和综合性能全面评定。CEIDI西递设计团队经常在设计提案的时候反复强调生物洁净室是为了防止污染和消灭微生物而建立的,因此对其设计时应进行负荷计算和能耗分析以此达到指定的净化功能,从经济和实用角度来说既要满足规范也不能完全搬套,成熟的做法是按照工艺需求和预算适度精简平面,以达到安全、实用、经济、可行的目的。除了尽合理分区、洁污分开,人/流动线不迂回等设计思路,遇到面积吃紧的厂区要紧凑规划的,CEIDI西递也坚持在缓冲间的设计上多做考量,有些场合下更衣和洁具间也可同步用作缓冲功能。生物制剂的生产车间要有无菌环境,在装修之前要划分好清洁区、半清洁区和辅助区。

生物制药车间洁净室的设计装修要点 CEIDI西递
1、核心检测部分和核心工艺部分按工作流程配置一更、二更、风淋和缓冲等实验前的准备工作。采用人流、物流分开原则减少污染 。
2、洁净室入口处设置风淋室,除了吹淋功能也起到了气闸的作用,防止不洁净空气由门进入洁净区。
3、以冻干工艺为例,对环境要求比较高。灌装、半加塞、冻干过程中制品处于完全未密封状态下的转运、直接接触药品的包装材料、器具灭菌后的装配、存放以及处于未完全密封状态下的转运,洁净室内环境要设置到B级背景下的A级范围;冻干过程中制品处于完全微密封状态下的产品置于完全密封容器内转运、直接接触药品的包装材料、器具灭菌后处于密封容器内的转运及存放,这类洁净室要设置为B级。
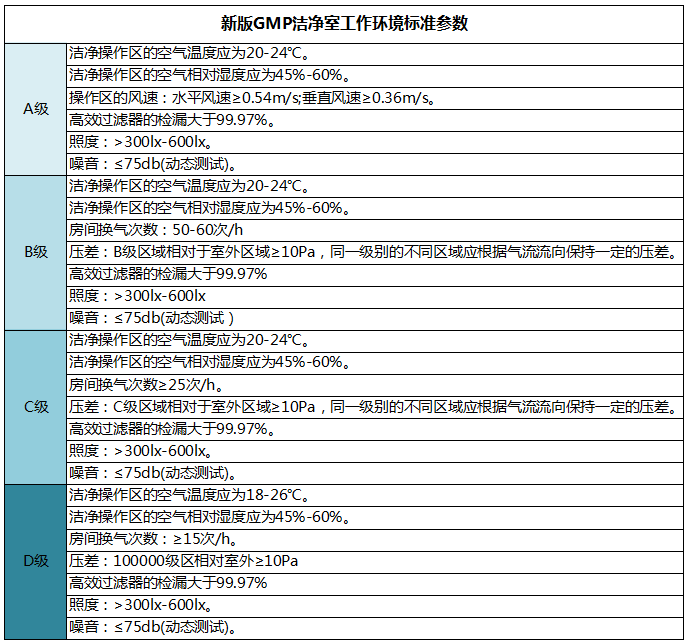
4、像B+A级高风险有毒区域设计人流物流,要考虑人员进入时与退出时的更衣净化通道完全分开,回更、退更更衣环境最大限度地减少更衣程序造成的交叉污染,同时保证非活性区域不受活性区域的影响。
5、生物药(例如干细胞制剂)在工艺流程设计中有隔离系统或者密闭自动制备系统的洁净室环境采用C+A即可。有来源于暴露于外环境的组织(如脐带、胎盘等),CEIDI建议要设计独立的预处理间,检测合格后再进入生产制备区。
6、在洁净室气流组织设计方面,生物洁净室的气流组织设计要依据工艺要求满足各生产区域内的通风和排气需要,保证气流组织设计、气流分布不影响净化室内的空气质量,使气流分布均匀、送风顺畅;同时在各生产区域内,推荐设置单向流,使整个生产空间形成单向流,从而减少由于室内流动方向变化而引起的压差。
7、关于自控及监控,生物药制备很多区域需进行实时的在线粒子监控,评估和控制生产过程中产生的颗粒的影响(例如:拆内包工艺环节)。为降低微生物污染风险,一般会设置自动拆内包的生产工序,需要良好的自控系统配置。在装修设计中布线、配电柜、USP电源等工程设施要注意避免迂回与节能设计。
8、管线组织适合与各类机房的布置一起规划,采取不同的隐蔽措施。如管道竖井作为各类管线竖向集中空间, 建议与机房相邻布置。技术夹层作为管线水平分散空间, 要为管线地穿行及检修提供足够的空间。
……
生物制品洁净厂房由于药物品种的特殊性,决定了工艺流程设计的复杂性和公用系统的建设难度。血液制品、疫苗、重组蛋白、单克隆抗体这些不同类目药物的生产工艺决定了不同洁净厂房设计的特殊性。针对生物药品研究/生产场所建设及对技术要求咨询的需求,欢迎有相关需求的企业联系CEIDI西递进行咨询,咨询热线:021-62250299,400-666-1693。
主要参考规范:
《实验室生物安全通用要求》GB19489-2004、
《微生物和生物医学实验室生物安全通用准则》WS233-2002、
《生物安全实验室建筑技术规范》GB50346-2004、
《洁净厂房设计规范》GB50073-2001、
《洁净室施工及验收规范》JGJ71-90、
《通风与空调工程施工及质量验收规范》、
《建筑安装工程技术操作规程通风空调》、
《建筑给水排水及采暖工程施工质量验收规范》、
《民用建筑电气设计规范》
项